
- Muallif Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Oxirgi o'zgartirilgan 2025-01-22 17:13.
The orasidagi farq uchta nazariya shundan iboratki Arrhenius nazariyasi shuni ta'kidlaydi kislotalar har doim H + ni o'z ichiga oladi va bu asoslar har doim OH- o'z ichiga oladi. esa Bronsted-Lowri model buni da'vo qilmoqda kislotalar proton donorlari va pron-akseptorlaridir asoslar OH-ni o'z ichiga olishi shart emas kislotalar H3O+ hosil qiluvchi suvga proton beradi.
Odamlar shuningdek, Bronsted Lowry kislotasi va asos o'rtasidagi farq nima?
The Bronsted - Lowry nazariyasi Kislotalar va asoslar A Bronsted - Lowry kislotasi proton (vodorod ioni) donori hisoblanadi. A Bronsted - Lowry bazasi proton (vodorod ioni) qabul qiluvchi hisoblanadi.
Keyinchalik savol tug'iladi: Arrhenius ta'riflari bilan bog'liq asosiy muammo nima? (Qoidadan istisnolar kamchiliklarga olib keladi Arrhenius qonuni) Kislotalar H2O da eriganida gidroniy ionlarini hosil qiladi. PH 7 dan kam. Asoslar H2O da eritilganda gidroksid ionlarini hosil qiladi.
Bundan tashqari, Arrhenius tomonidan kislota va asosning ta'rifi nima?
Sifatida belgilangan tomonidan Arrhenius , kislota - asos reaksiyalar bilan tavsiflanadi kislotalar , ular suvli eritmada vodorod ionlarini hosil qilish uchun ajraladi (H+) va asoslar , ular gidroksid hosil qiladi (OH−) ionlari. Kislotalar bor belgilangan vodorodni chiqaradigan birikma yoki element sifatida (H+) ionlari eritmaga (asosan suv).
Kislotalar va asoslarning uchta ta'rifi qanday?
Lar bor uch deb nomlanuvchi moddalarning asosiy tasniflari kislotalar yoki asoslar . Arrhenius ta'rifi ta'kidlaydiki, an kislota H ishlab chiqaradi+ eritmada va a asos OH hosil qiladi-. Bular Bronsted-Lowry va Lyuislar kislotalar va asoslarning ta'riflari.
Tavsiya:
PH shkalasi bo'yicha kislotalar va asoslar o'rtasidagi farq nima?

Kislota va asoslarni farqlash. Asosiy farq: Kislotalar va asoslar ikki turdagi korroziy moddalardir. pH qiymati 0 dan 7 gacha bo'lgan har qanday modda kislotali hisoblanadi, apH qiymati esa 7 dan 14 gacha bo'lgan modda asos hisoblanadi. Kislotalar suvda parchalanib, vodorod ionini (H+) hosil qiluvchi ionli birikmalardir
Misollar bilan tezlik va tezlik o'rtasidagi farq nima?
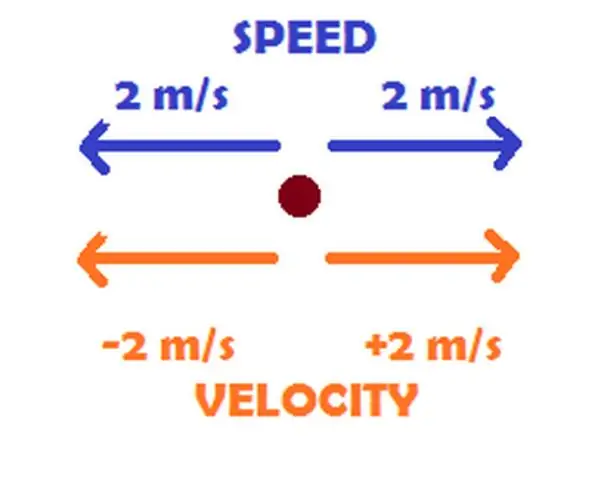
Sababi oddiy. Tezlik - bu jismning yo'l bo'ylab harakatlanadigan vaqt tezligi, tezlik esa ob'ekt harakatining tezligi va yo'nalishi. Masalan, 50 km/soat (31 milya) avtomobil yo‘l bo‘ylab harakatlanayotgan tezligini, g‘arbga esa 50 km/soat uning harakatlanish tezligini tavsiflaydi
Misollar bilan zichlikka bog'liq bo'lmagan va zichlikka bog'liq omillar o'rtasidagi farq nima?

U katta va kichik populyatsiyalarda ishlaydi va aholi zichligiga asoslanmaydi. Zichlikka bog'liq omillar - bu aholining zichligiga qarab o'sishini tartibga soluvchi omillar, zichlikka bog'liq bo'lmagan omillar esa aholining zichligiga bog'liq bo'lmagan holda o'sishini tartibga soluvchi omillardir
Bazaning Bronsted Louri ta'rifi qaysi?

Bronsted-Lowri kislotasi - bu reaktsiyada bir yoki bir nechta vodorod ionlarini beradigan kimyoviy tur. Bundan farqli o'laroq, Bronsted-Lowry bazasi vodorod ionlarini qabul qiladi. U o'z protonini berganida, kislota uning konjugat asosiga aylanadi. Nazariyaga umumiy nuqtai nazar, proton donori sifatida kislota va proton qabul qiluvchi sifatida asosdir
Bronsted Louri nazariyasiga ko'ra kislotalar va asoslar nima?

1923 yilda kimyogarlar Yoxannes Nikolaus Bronsted va Tomas Martin Louri birikmalarning protonlarni (H+ ionlarini) berish yoki qabul qilish qobiliyatiga asoslangan holda kislotalar va asoslarning ta'riflarini mustaqil ravishda ishlab chiqdilar. Bu nazariyada kislotalar proton donorlari sifatida aniqlanadi; bazalar esa proton qabul qiluvchilar sifatida aniqlanadi
