
- Muallif Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Oxirgi o'zgartirilgan 2025-01-22 17:12.
Faollashtirish energiyasi - bu a uchun so'rilishi kerak bo'lgan energiya miqdori kimyoviy reaksiya boshlamoq. Reaktivlarga yetarlicha faollashtirish energiyasi qo‘shilsa, obligatsiyalar reaktivlarda tanaffus va reaktsiya boshlanadi.
Bu erda kimyoviy reaktsiyalar paytida aloqalar qanday uziladi va hosil bo'ladi?
Kimyoviy reaksiyalar energiyani chiqaradi yoki yutadi. Reaktivlarga qo'shiladigan energiya tanaffuslar ularning kimyoviy bog'lanishlar . Yangi qachon obligatsiyalar hosil qiladi mahsulotlarda energiya ajralib chiqadi. Bu shuni anglatadiki, energiya ham so'riladi, ham chiqariladi davomida a kimyoviy reaksiya . Biroz kimyoviy reaksiyalar ular o'zlashtirganidan ko'ra ko'proq energiya chiqaradi.
Ikkinchidan, obligatsiyalar qayerda buziladi? Reaksiyada olingan yoki chiqarilgan issiqlik kimyoviy moddadan kelib chiqadi obligatsiyalar qilinmoqda yoki buzilgan reaktsiyada. Kimyoviy reaksiya davomida, agar zarur bo'lgan umumiy energiya aloqalarni buzish reaktivlarda yangi bo'lganda chiqarilgan umumiy energiyadan ko'proq obligatsiyalar mahsulotlarda hosil bo'ladi, bu endotermik reaksiya.
Keyinchalik savol tug'iladi: kimyoviy bog'lanish qachon uziladi energiya?
Bond - sindirish endotermik jarayondir. Energiya yangi bo'lganda chiqariladi obligatsiyalar shakl. Bond - yasash ekzotermik jarayondir. Reaksiyaning endotermik yoki ekzotermik bo'lishi reaksiyalar orasidagi farqga bog'liq energiya buzish kerak edi obligatsiyalar va energiya yangi bo'lganda chiqariladi obligatsiyalar shakl.
Kimyoviy bog'lanishning uzilishiga nima sabab bo'ladi?
Bond energiya - bu energiya miqdori tanaffuslar a rishta . ga energiya qo'shiladi aloqalarni buzish va qachon energiya ham chiqariladi obligatsiyalar shakl. Ekzotermik reaktsiyada mahsulotlar reaktivlarga qaraganda (ko'proq yoki kamroq) energiyaga ega.
Tavsiya:
Hujayra nafasi hujayraning qaysi qismida sodir bo'ladi?
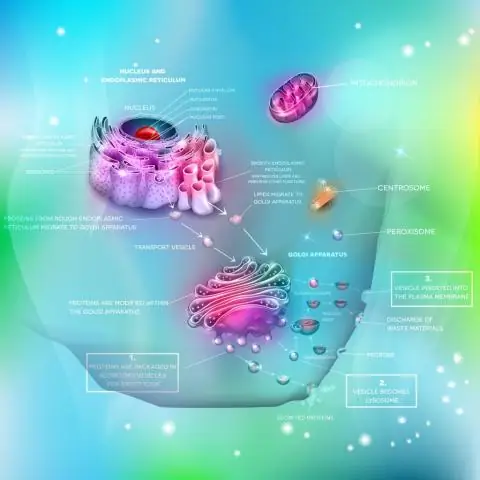
Mitoxondriyalar
Kimyoviy reaksiyaning entalpiyasi nima?

Reaksiya entalpiyasi. Kimyoviy reaktsiyalar paytida atomlar orasidagi aloqalar uzilishi, isloh qilinishi yoki ikkalasi ham energiyani o'zlashtirishi yoki chiqarishi mumkin. Doimiy bosim ostida tizimdan so'rilgan yoki chiqariladigan issiqlik entalpiya deb nomlanadi va kimyoviy reaktsiya natijasida yuzaga keladigan entalpiyaning o'zgarishi reaksiya entalpiyasidir
Nol tartibli reaksiyaning yarimparchalanish davri uning tezlik konstantasi bilan qanday bog‘liq?

Nol tartibli kinetikada reaksiya tezligi substrat konsentratsiyasiga bog'liq emas. Nol tartibli reaksiya uchun t 1/2 formulasi yarim yemirilish davri boshlang‘ich kontsentratsiya miqdori va tezlik konstantasiga bog‘liqligini ko‘rsatadi
Qaysi elementlar kimyoviy bog'lanishda elektron olish ehtimoli ko'proq?

Nometalllar Noble Gas konfiguratsiyasiga erishish uchun elektronlarni olishga moyildirlar. Ular nisbatan yuqori elektronga yaqinlik va yuqori ionlanish energiyasiga ega. Metalllar elektronlarni yo'qotishga moyil bo'lib, metall bo'lmaganlar esa elektron oladilar, shuning uchun bu ikki guruh ishtirokidagi reaktsiyalarda metalldan metall bo'lmaganga elektron o'tadi
Kimyoviy reaksiyaning dalili nima?

Rang o'zgarishi, cho'kma yoki gaz hosil bo'lishi yoki haroratning o'zgarishi kimyoviy reaktsiyaning dalilidir
