
- Muallif Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Oxirgi o'zgartirilgan 2025-01-22 17:12.
Xlor izotop 18 neytron bilan 0,7577 ko'pligi va 35 amu massa soniga ega. Hisoblash uchun o'rtacha atom massasi, kasrni har biri uchun massa soniga ko'paytiring izotop , keyin ularni birga qo'shing.
Xuddi shunday, elementning barcha izotoplarining o'rtacha og'irligi qancha?
Turli xil massalardan foydalanish izotoplar va har biri qanchalik ko'p izotop ni topishimiz mumkin o'rtacha a atomlarining massasi element . A ning atom massasi element bo'ladi vaznli o'rtacha tabiiy ravishda uchraydigan namunadagi atomlarning massasi element . Atom massasi odatda atom massa birliklarida qayd etiladi.
1 amu massasi nimaga teng? Atom massa birligi (ramzlangan AMU yoki amu) uglerod-12 atomi massasining 1/12 qismi sifatida aniqlanadi. Uglerod-12 (C-12) atomida oltita bor protonlar va olti neytronlar uning yadrosida. Aniq bo'lmagan holda, bitta AMU o'rtacha hisoblanadi proton dam olish massasi va neytron dam olish massasi.
Ikkinchidan, atom massasi yordamida foiz ko'pligini qanday hisoblash mumkin?
Har birini o'zgartiring foiz ko'pligi 100 ga bo'lish orqali o'nlik shaklga o'tkazing. Bu qiymatni ko'paytiring atom massasi bu izotopdan. O'rtachani olish uchun har bir izotop uchun qo'shing atom massasi.
Atom massasi va atom og'irligi o'rtasidagi farq nima?
Atom massasi (ma) bo'ladi massa ning atom . Bitta atom proton va neytronlarning belgilangan soniga ega, shuning uchun massa Bu aniq (o'zgarmaydi) va proton va neytronlar sonining yig'indisidir. atomda . Atom og'irligi ning o'rtacha og'irligi hisoblanadi massa hammasidan atomlar izotoplarning ko'pligiga asoslangan elementning.
Tavsiya:
Ikki tezlikda o'rtacha tezlikni qanday topasiz?
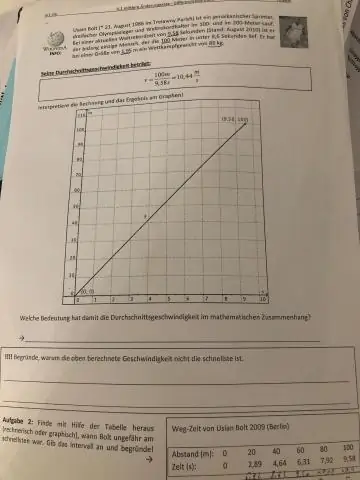
O'rtachani topish uchun boshlang'ich va oxirgi tezlik yig'indisi 2 ga bo'linadi. O'rtacha tezlik kalkulyatori o'rtacha tezlikni (v) yakuniy tezlik (v) va boshlang'ich tezlik (u) yig'indisi 2 ga bo'linganligini ko'rsatadigan formuladan foydalanadi
O'rtacha berilganda etishmayotgan raqamni qanday topasiz?

Raqamlar to'plamining o'rtacha qiymati bu raqamlarning o'rtachasidir. Raqamlar to'plamini qo'shish va berilgan nechta songa bo'lish orqali mavzuni topishingiz mumkin. Agar sizga mavzu berilsa va to'plamdan etishmayotgan raqamni topish so'ralsa, oddiy tenglamadan foydalaning
O'rtacha nisbatni qanday topasiz?
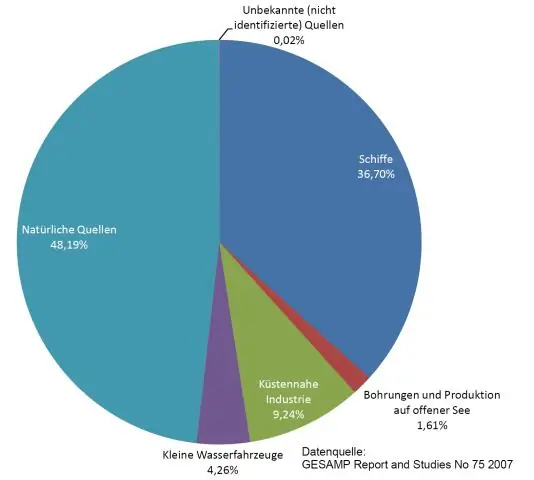
O'rtacha proportsionalni topishning yo'li ikkita sonni birga ko'paytirish, keyin ularning kvadrat ildizini topishdir. Bu o'rtacha proportsional bo'ladi
O'rtacha bepul yo'lni qanday topasiz?

O'rtacha erkin yo'l - bu molekulaning to'qnashuvlar orasidagi masofa. O'rtacha erkin yo'l "to'qnashuv trubkasi" ichida molekulyar traektoriya bilan chiqarib yuborilgan bitta molekula mavjudligi mezoni bilan aniqlanadi. Mezon: λ (N/V) π r2 ≈ 1, bu erda r - molekula radiusi
Jadvaldagi o'rtacha va medianni qanday topasiz?
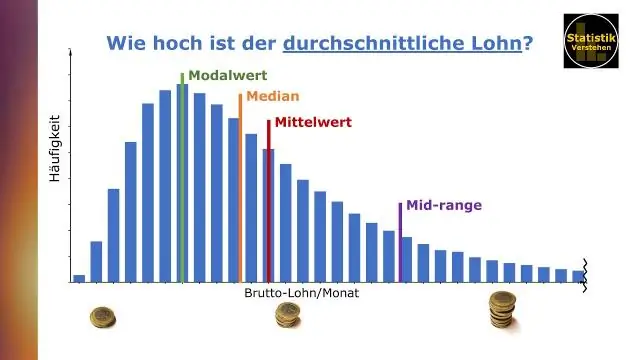
Ben Jons tomonidan Tableau bilan ma'lumotlarni bog'lash O'rtacha (yoki o'rtacha) ma'lumotlar to'plamidagi barcha qiymatlarni yig'ish va qiymatlar soniga bo'lish yo'li bilan aniqlanadi. Median ma'lumotlar to'plamidagi o'rta qiymat bo'lib, unda qiymatlar kattalik tartibida joylashtirilgan
